自然界中的一切生命现象都与酶息息相关。人们所熟知的天然酶主要由蛋白质构成,具有底物专一,催化效率高的特点。然而,由于大多数天然酶在酸、碱、热等非生理条件下,容易发生结构变化而失去活性,且制备繁琐、价格昂贵。这些缺点很大程度上限制了天然酶的实际应用。为了解决上述问题,人们一直努力寻找和探索新型的天然酶替代物。自 2007 年阎锡蕴院士发现四氧化三铁纳米粒子具有辣根过氧化物酶(HRP)类似活性后,纳米酶的概念应运而生。纳米酶通常是在纳米尺度上,能呈现出酶学特性的无机材料。与天然酶类似,能在温和的生理条件下高效催化酶的底物,产生与天然酶相同的反应产物,并可作为酶的替代品调节细胞代谢,用于疾病的诊断和治疗。纳米酶的问世,改变了以往人们认为无机纳米材料是一种生物惰性物质的传统观念,揭示了纳米材料内在的生物效应及新特性。在短短十年间涌现出许多关于纳米酶的研究,研究的涉及面也逐渐扩展至材料科学、物理、化学、生物、医学和环境等不同领域。
纳米酶的种类大致可归纳为三类:(1)贵金属纳米材料。如,金纳米颗粒和纳米棒、铂纳米颗粒以及多金属形成的复合纳米材料。如金铂纳米棒、银(铂、金、钯)纳米颗粒等;(2)金属氧化物纳米材料。如,Fe3O4 、Fe2O3、铁铋氧化物纳米粒、铁钴氧化物纳米粒和铁锰氧化物纳米粒等,此外一些金属硫化物如硫化铜纳米粒,硫化镉,硫化亚铁等纳米粒也具有类似的催化活性;(3)非金属纳米酶,尤其是碳基纳米材料也具有过氧化物酶活性。如,碳纳米管、氧化石墨烯、碳纳米点等。
目前发现的纳米酶表现出的模拟酶活性主要包括 4 类:(1)氧化酶(oxidase, OXD),在酸性条件下可以直接催化氧气产生自由基;(2)过氧化物酶(peroxidase, POD),酸性条件下催化双氧水产生羟基自由基;(3)过氧化氢酶(catalase, CAT),中性条件下将双氧水分解为氧气和水;(4)超氧化物歧化酶(superoxide dismutase, SOD),中性或碱性条件下将超氧自由基氧化为氧气或双氧水。氧化酶和过氧化物酶催化产生自由基,表现为提高活性氧(ROS)水平;而过氧化氢酶和超氧化物歧化酶清除自由基,表现为降低 ROS 水平。因此纳米酶具有调节ROS 水平的能力。例如:纳米酶进入细胞后,如果进入溶酶体酸性环境中,它将以过氧化物酶活性为主,提高 ROS 水平;如果进入细胞质中性环境区域,将以过氧化氢酶活性为主,表现为降低 ROS 水平。因此可以基于实验目的的需要将纳米酶运送到相应的细胞内微环境,发挥特定的作用。
最近,利用纳米酶引发自由基风暴的特点,打破生物体系的ROS的平衡,破坏细胞膜的完整性,最终引发细胞发生剧烈变化并导致死亡的策略,已经被用于肿瘤的治疗。扬州大学医学院高利增课题组与中国科学院生物物理研究所阎锡蕴课题组最新的研究成果显示通过对纳米酶多酶体系的体内活性调控,可以将肿瘤代谢产物催化为毒性物质,实现对肿瘤的特异性杀伤。
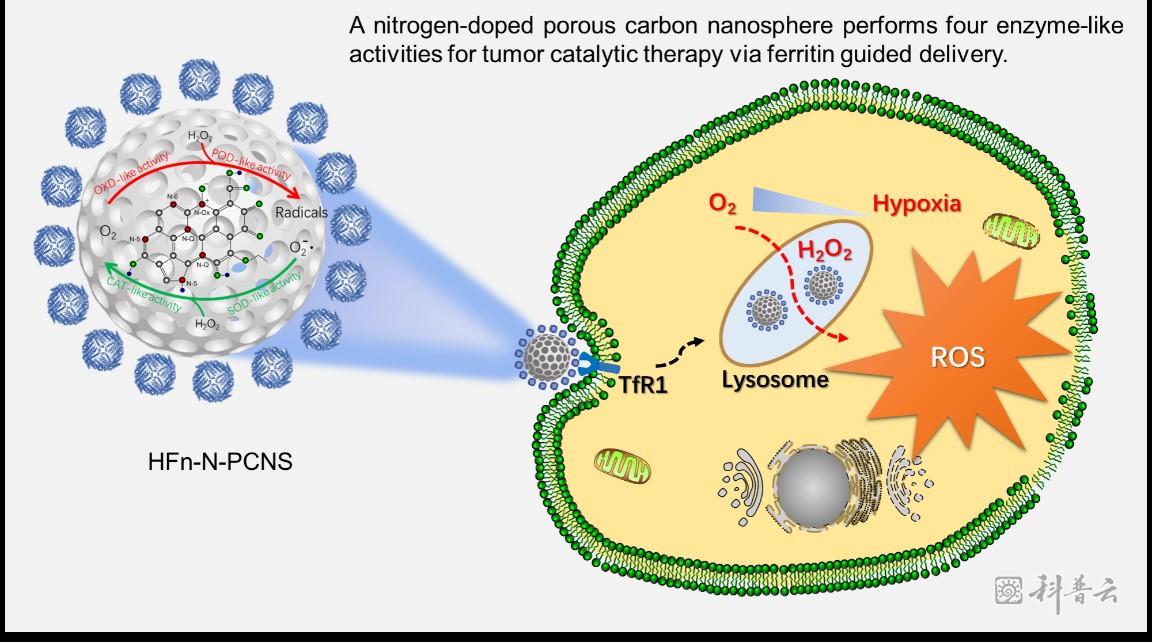
碳纳米酶用于肿瘤治疗(图片来自网络)
肿瘤代谢具有与正常细胞不同的特征,例如,肿瘤细胞会积累大量的过氧化氢。如何利用肿瘤代谢产物发展“以彼之道,还施彼身”的肿瘤治疗策略是肿瘤生物治疗的新领域。由于过氧化氢可被过氧化物酶催化产生具有细胞毒性的自由基,因此过氧化物酶被寄予开发肿瘤新药物的希望。但是天然酶往往稳定性较差,在复杂的体内环境中容易失活,因而其应用受到限制。文章探索了兼具酶催化活性和纳米材料稳定性的纳米酶在该策略中的应用。实验中首先设计合成了具有氧化酶、过氧化物酶、过氧化氢酶及超氧化物歧化酶四种酶活性的新型纳米酶。这种新型纳米酶在酸性条件下,发挥氧化酶和过氧化物酶活性,可催化氧气和过氧化氢产生活性氧自由基;在中性环境下则主要表现为过氧化氢酶和超氧化物歧化酶活性,可以清除自由基,并利用铁蛋白对这种新型碳氮纳米酶进行修饰,并通过实验验证了铁蛋白修饰后的碳氮纳米酶可以特异识别肿瘤细胞,并定位于肿瘤细胞内部具有酸性环境的溶酶体中,其氧化酶和过氧化物酶被特异性激活,催化肿瘤内的氧气和过氧化氢产生高毒性的活性氧自由基,实现对肿瘤细胞的特异性杀伤。动物荷瘤实验表明,铁蛋白-纳米酶可显著抑制肿瘤的生长。
纳米酶的出现,拓宽了人们对于模拟酶的认知,使得模拟酶的研究不再局限于有机小分子的设计与合成,其生物催化特性,已用于检测小分子、核酸、蛋白质、癌细胞等,此外,纳米酶还可以用于污水处理、疾病治疗等领域。此外,纳米酶在疾病治疗领域的研究还处在初级阶段,而且材料本身的生物毒性也限制了其在生物医学上的潜在应用。因此,探索新型高效及生物安全性好的纳米酶并将其应用于炎症、癌症、神经退行性疾病等治疗领域将会是今后研究的热点。